Elektrofil tilsætning i organisk kemi
Vedhæftningsreaktionerne er kendetegnet ved dannelsen afen kemisk forbindelse fra to eller flere af udgangsmaterialerne. Overvej mekanismen for elektrofiltilsætning er praktisk for eksemplet af alkener - umættede acykliske carbonhydrider med en dobbeltbinding. Bortset fra disse indtræder andre carbonhydrider med flere bindinger, herunder cykliske, sådanne transformationer.
Trin af interaktion mellem indledende molekyler
Elektrofile sammenføjninger finder sted i flereetaper. Elektrofilen, som har en positiv ladning, virker som en elektronacceptor, og alkenmolekylets dobbeltbinding spiller rollen som en elektrondonor. Begge forbindelser danner først et ustabilt p-kompleks. Så begynder transformationen af π-komplekset i ϭ-komplekset. Dannelsen af carbocation på dette stadium og dens stabilitet bestemmer hastigheden af interaktion som helhed. Efter dette interagerer carbocation hurtigt med en delvist negativt ladet nukleofil, og slutproduktet af transformation dannes.

Virkningen af substituenter på reaktionshastigheden
Delokalisering af ladningen (ϭ +) i carbocationfra strukturen af det oprindelige molekyle. Den positive induktive virkning, som alkylgruppen udviser, fører til en lavere ladning af det nærliggende carbonatom. Som et resultat, i molekylet med elektrondonerende substituent forøger den relative stabilitet i kation π-elektron densitet skyldes og reaktivitet af molekylet som helhed. Effekten af elektronacceptorer på reaktivitet vil være modsat.
Mekanismen for halogenaddition
Lad os analysere mere detaljeret mekanismen for reaktionen af elektrofiltilsætning ved eksemplet af interaktionen mellem alken og halogen.
- Halogenmolekylet nærmer sig en dobbeltbindingmellem carbonatomer og polariseres. På grund af en delvist positiv ladning i den ene ende af molekylet trækker halogenet π-bindingselektroner. Sådan dannes det ustabile π-kompleks.
- I det næste trin kombinerer den elektrofile partikel med to carbonatomer for at danne en cyklus. En cyklisk "onium" ion vises.
- Den resterende ladede halogenpartikel(en positivt ladet nukleofil) interagerer med en oniumion og er forbundet på den modsatte side af den foregående halogenpartikel. Slutproduktet, trans-1,2-dihalogenalkan, fremkommer. Tilsvarende tilsættes halogen til cycloalken.
Mekanismen for tilsætning af hydrogenhalogenidsyrer
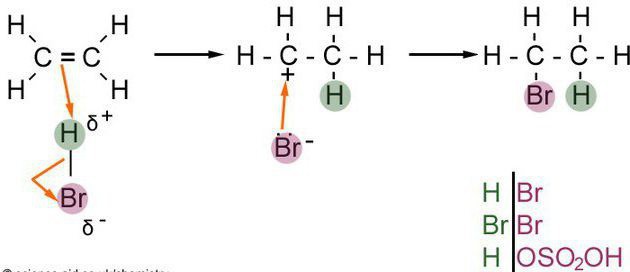
Elektrofile additionsreaktionerHydrogenhalogenider og svovlsyre fortsætter forskelligt. I et surt medium dissocieres reagenset i en kation og en anion. En positivt ladet ion (elektrofil) angriber π-bindingen, kombinerer med et af carbonatomerne. En carbocation-form, hvori det nærliggende carbonatom er ladet positivt. Yderligere reagerer carbocation med anionen for at danne det endelige reaktionsprodukt.
Reaktionen af reaktionen mellem asymmetriske reagenser og Markovnikov-reglen

Elektrofil vedhæftning mellem toasymmetriske molekyler fortsætter regioselektivt. Dette betyder, at kun en af de to mulige isomerer er dannet. Regioselektivitet beskriver Markovnikov regel, hvorefter hydrogenet er bundet til et carbonatom forbundet med en lang række andre hydrogenatomer (mere hydrogeneret).
For at forstå essensen af denne regel skal vi huskeat reaktionshastigheden afhænger af stabiliteten af den mellemliggende carbokation. Påvirkningen af elektron-donor- og acceptorsubstituenter blev diskuteret ovenfor. Således vil elektrofil tilsætning af brombrintesyre til propen resultere i dannelsen af 2-brompropan. En mellemliggende kation med en positiv ladning på et centralt carbonatom er mere stabilt end en carbokation med en positiv ladning ved det ekstreme atom. Som et resultat interagerer bromatom med det andet carbonatom.

Effekt af elektron-udtagende substituent på interaktionsforløbet
Hvis kilde molekylet indeholderelektrontiltrækkende substituent, der har en negativ induktiv og / eller mesomere virkning, elektrofil addition er imod ovennævnte regler. Eksempler på sådanne substituenter er CF3, COOH, CN. I dette tilfælde jo større afstand af den positive ladning af den primære elektrontiltrækkende gruppe gør en mere stabil carbokation. Som et resultat kombinerer hydrogen med et mindre hydrogeneret carbonatom.
Universel version af reglerne vil se sådan ud: vekselvirkningen af en asymmetrisk alken og en asymmetrisk reagens Reaktionen forløber i form af dannelsen af det mest stabile carbokation.







